据世界卫生组织报道,全球有超过 10 亿人患有肥胖症[1]。而在中国,有 34.8% 的人超重,14.1% 的人肥胖[2]。2023 年 GLP-1R 激动剂在对抗肥胖及相关病症中取得了令人瞩目的成功,同时临床试验发现 GLP-1R 激动剂对心脏、大脑等均有益处,被 Science 评为年度突破成果[3]。

GLP-1 (Glucagon-like peptide-1) 是一种主要由肠道 L 细胞分泌的肠促胰素,可以激活 GLP-1 受体 (GLP-1R),以葡萄糖浓度依赖的方式促进胰岛素释放、抑制胰高血糖素分泌,从而达到降低血糖、减肥等作用[4][5]。
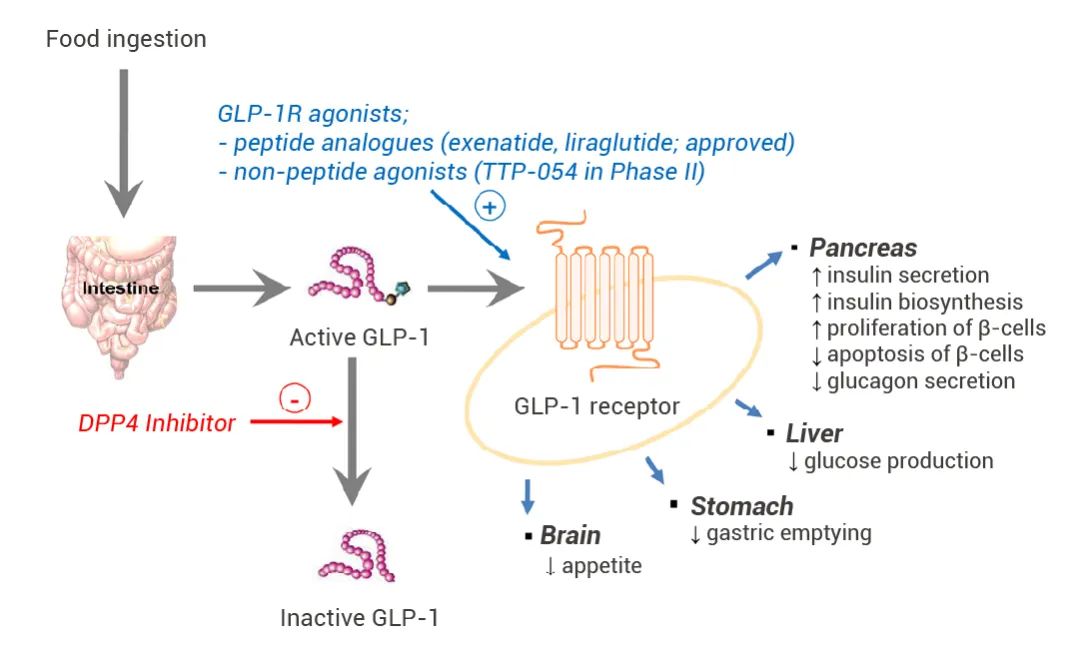
图 1. GLP-1 对胰腺及其它组织的生理作用[6]。
营养摄入会刺激 GLP-1 的分泌,GLP-1 通过与 GLP-1R 结合发挥作用,这种结合会激活腺苷酸环化酶,导致 cAMP 及 PKA 升高,最终增加胰岛素的生物合成与分泌,并抑制 α 细胞分泌胰高血糖素[5]。除胰腺外,GLP-1R 还广泛分布于肾脏、心脏、肺等组织中,因此 GLP-1 还具有促进胃排空、降低食欲、减少肝脏糖异生、降低心血管疾病等功能[4][6]。

受体激动剂是激活特定受体并引发反应的分子,可以是天然配体或模仿天然配体设计的分子。GLP-1 受体激动剂 (GLP-1RA) 通过激活 GLP-1R 发挥作用,主要被用于治疗 2 型糖尿病 (T2D) 与肥胖。
▐ 实验走向临床 —— 艾塞那肽的发现
19 世纪 80 年代 GLP-1 及其生理功能被发现后,科学家便基于 GLP-1 的活性形式 GLP-1(7-37) 及 GLP-1(7-36),amide 进行药物开发,而这两种天然的 GLP-1RA 会很快被 DPP-4 酶解,并在 1-2 min 内被肾脏清除,不具备直接成药性。
GLP-1 成药的问题困扰了科学家数年,直到 1992 年,科学家在 Gila monster 毒液中发现了艾塞那肽 (Exenatide),它与 GLP-1(7-37) 的同源性为 53%,可作为 GLP-1R 的激动剂,可以抗 DPP4 酶解且具有较低的人体肾脏清除率,成为第一个被成功开发的 GLP-1 药物[7]。
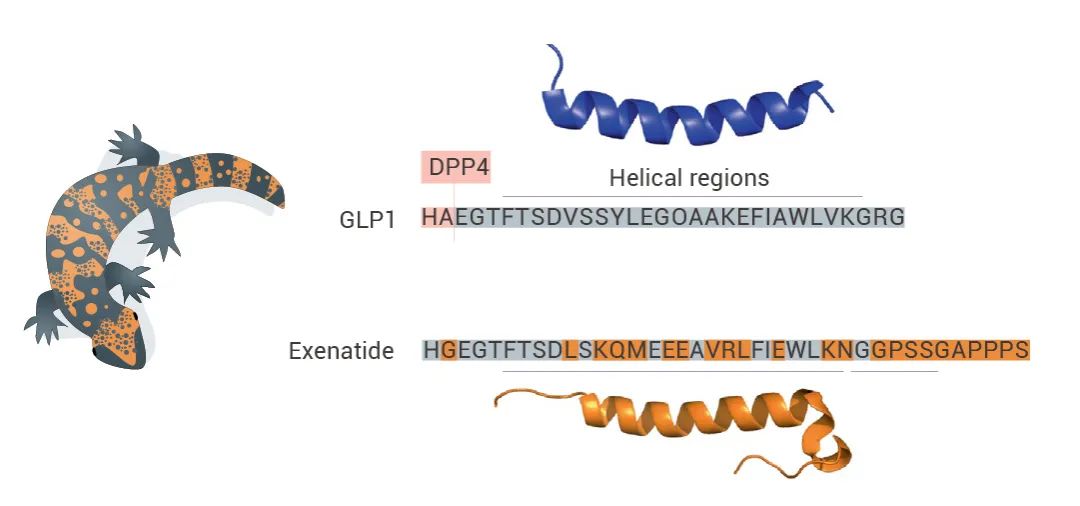
图 2. Gila monster 中分泌的 Exenatide 与 GLP-1(7-37) 序列的对比[7]。
▐ 里程碑式的 GLP-1RA —— 司美格鲁肽
基于 GLP-1 开发的多肽类药物因难以胃肠道给药,需要注射导致患者依从性降低,最终影响疗效。故在 Exentide 上市后 GLP-1 类药物的研发主要导向两个方向:开发长效 GLP-1RA 与口服 GLP-1RA(图 3)。
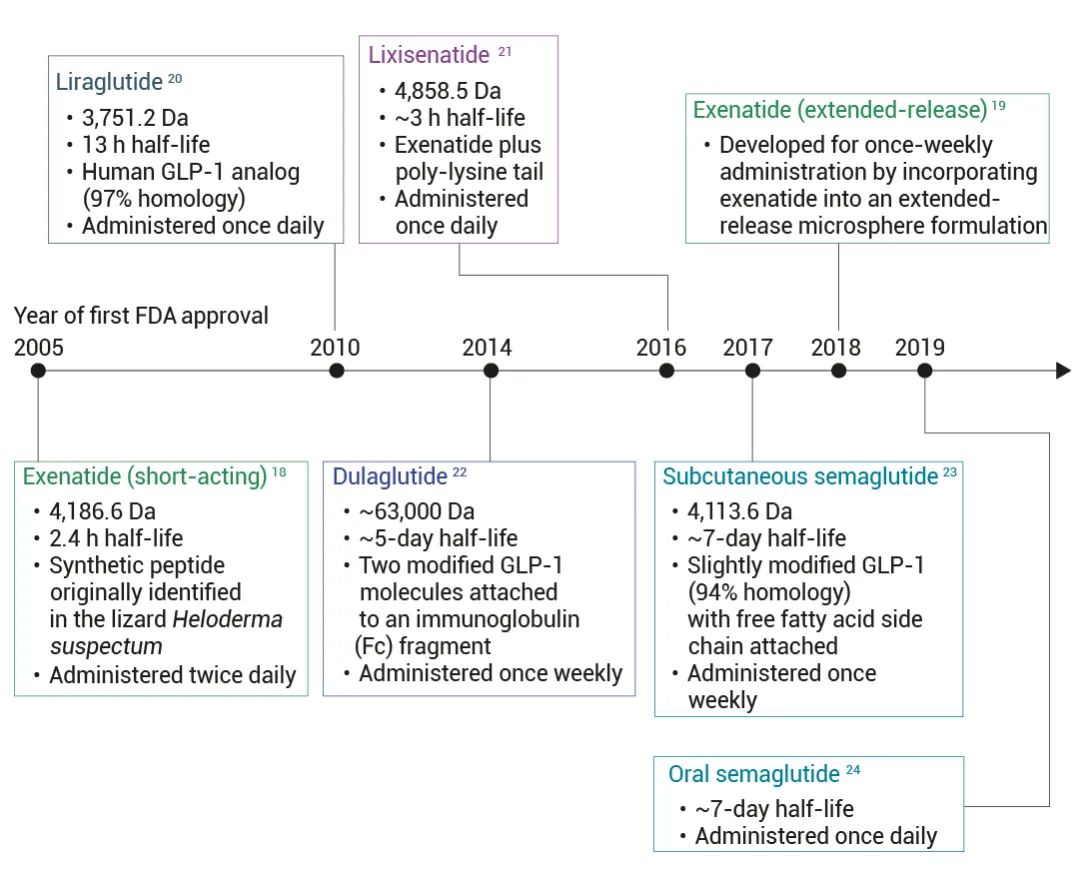
图 3. FDA 批准上市的 GLP-1RA[8]。
截至 2023 年第三季度,司美格鲁肽 (Semaglutide) 销售额一举迈入全球前三[9]。终端市场取得的成功彻底点燃了市场与科研工作者对肥胖的关注与对 GLP-1RA 类药物的研发热情。这种第二代 GLP-1RA 进一步挖掘了 GLP-1RA 在市场及科学上更多的可能性。
基于 GLP-1(7-37),司美格鲁肽在 Lys 侧链上修饰了长链脂肪酸,使其可与血浆白蛋白结合并在体内缓慢释放,同时将第 8 位及第 34 位氨基酸替换为 Aib 与 Arg,避免其被 DPP-4 酶降解并防止其在末端与脂肪酸进行错误结合,从而实现了半衰期的大幅延长 (7 天)。随后,Novo Nordisk 将司美格鲁肽与渗透促进剂 SNAC 配伍制剂进一步开发出口服剂型,也是第一个被 FDA 批准上市的口服 GLP-1RA[8][10]。
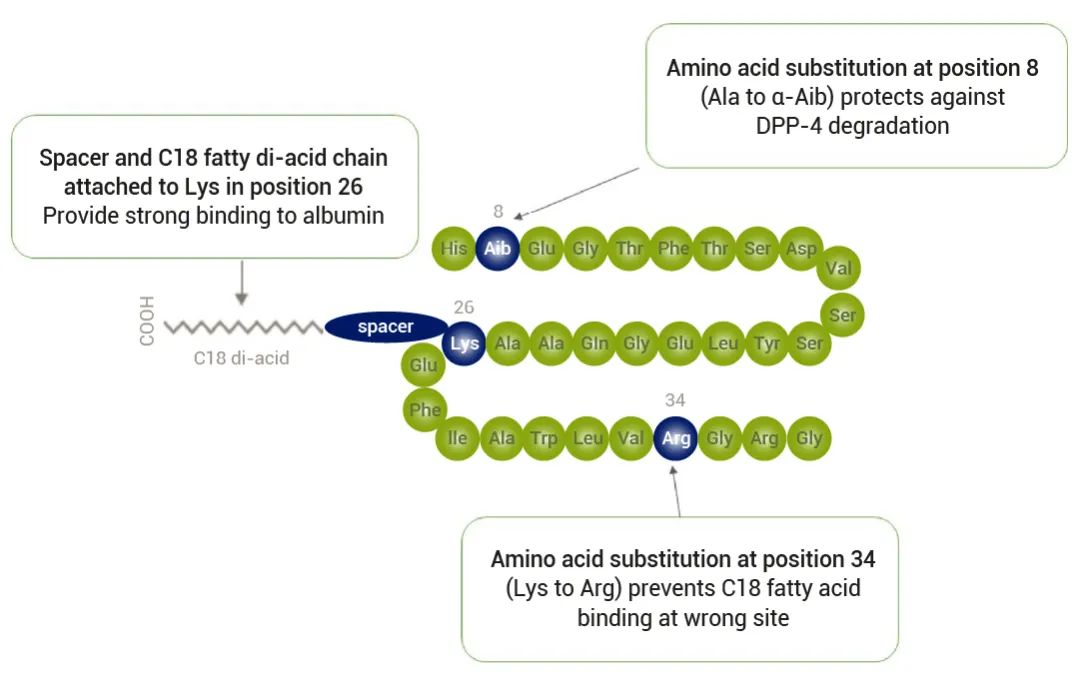
图 4. 司美格鲁肽的结构示意图[10]。
2021 年司美格鲁肽被 FDA 批准用于减肥,并迅速取得了巨大成功。连续使用司美格鲁肽可使体重在 68 周时减少约 15%,同时使心血管风险因素和身体机能也得到改善[11]。不止于 T2D 与肥胖,司美格鲁肽仍在积极扩展其他的适应症如心血管疾病、脂肪肝、慢性肾病等,目前都已进入 III 期临床,将 GLP-1RA 的影响力扩展到更多的医疗领域中。
▐ 创新发展 —— 多功能肽与 GLP-1RA 小分子
除去对 GLP-1RA 的适应症进行拓展外,前沿的 GLP-1RA 研究聚焦于发展多靶点的 GLP-1RA 激动剂及口服小分子类 GLP-1RA。
2009 年,Richard DiMarchi 与 Matthias H Tschöp 团队报道靶向 GLP-1R 与 GCGR 的双重激动剂相对 GLP-1RA 具备更好的减肥效果[12]。2014 年他们又报道了在小鼠实验中展示更佳疗效的 GLP-1R/GIPR/GCGR 的三重受体激动剂[13]。基于这些研究成果, Eli Lilly 成功开发出了靶向 GLP-1R/GIPR 的双重激动剂替尔泊肽 (Tirzepatide),于 2022 年被 FDA 批准上市,对 T2D 及肥胖均表现出良好的治疗效果。同公司研发的 GIP-1R/GIPR/GCGR 三重激动剂雷塔鲁肽(Retatrutide) 在 III 期临床中也表现了相对替尔泊肽更佳的减重效果。
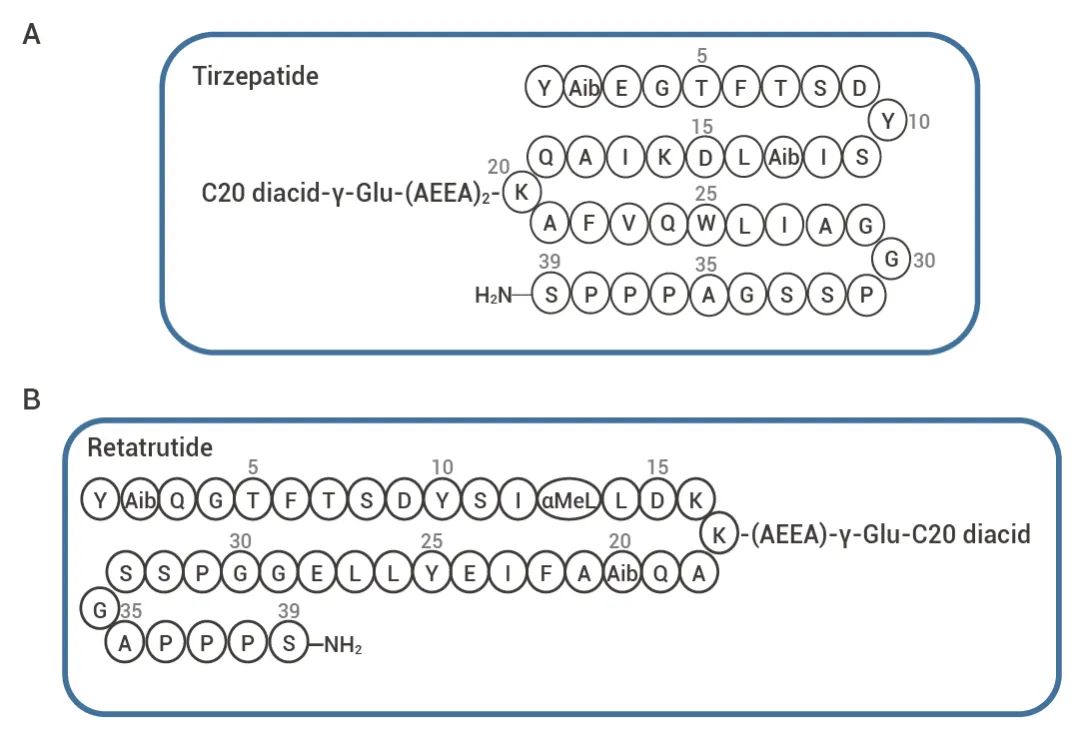
图 5. 替尔泊肽(上)与雷塔鲁肽(下)的结构示意图[14][15]。
基于 GLP-1R 开发的多功能肽展现了更佳的作用效果,但给药方式却较为受限。部分科研工作者则将目光转向于研发 GLP-1RA 小分子——口服生物利用率高、给药不受饮食饮水影响、患者依从性高。这条崭新的赛道尚没有幸运儿脱颖而出,Orforglipron 是其中暂时的一位明星选手,实验显示 Orforglipron 表现出良好的血糖控制及体重管理效果[16][17]。GLP-1RA 小分子的发展为长期接受注射治疗的超重及 T2D 患者提供了新的选择。
GLP-1RA 在控制血糖及体重管理的临床实践中都取得了令人瞩目的成果,尽管 GLP-1RA 的长期安全性其对其它适应症(如肾病、脂肪肝等)的疗效仍待验证,但 GLP-1RA 为肥胖及相关疾病带来了更多的社会关注与科研投入,将进一步推动相关代谢疾病的科学发展与医学突破。
相关产品
|
GLP-1(7-36), amide acetate
GLP-1(7-36), amide acetate 是一种主要的肠道激素,在葡萄糖的刺激下,它能促使胰岛 β 细胞分泌胰岛素。
|
|
GLP-1(7-37)
GLP-1(7-37) 是一种肠道胰岛素激素,可以增强葡萄糖诱导的胰岛素分泌。
|
|
Exendin-4
Exendin-4 是长效的 glucagon-like peptide-1 受体激动剂。
|
|
Exendin(9-39) amide
Exendin (9-39) 是特异竞争性的 glucagon-like peptide-1 (GLP-1) 受体拮抗剂。
|
|
Insulin (human)
Insulin (human) 是一种多肽激素,可以调节血液中的葡萄糖水平。
|
|
CD26/Dipeptidyl Peptidase 4 蛋白, Human (HEK293)
Dipeptidyl Peptidase 4(二肽基肽酶-4)是一种丝氨酸外肽酶,可选择性地从多种底物中切割 N 端二肽。DPP-4 通过裂解 GLP-1 调节葡萄糖稳态。
|
|
GLP1R 蛋白, Human (HEK293, Fc)
GLP1R 是 GLP-1 的受体, GLP-1 通过与 GLP-1R 结合,触发一系列信号传导通路,参与葡萄糖稳态调节。
|
|
GLP-1R modulator C16
GLP-1R modulator C16 是一种变构调节剂,通过跨膜位点增强 GLP-1 与 GLP-1R 的结合。
|
| |
MCE的所有产品仅用作科学研究或药证申报,我们不为任何个人用途提供产品和服务。
参考文献:
[1] World Obesity Day 2022 – Accelerating action to stop obesity. WHO news. 2022 Mar 4.
[2] Chen K, et al. Prevalence of obesity and associated complications in China: A cross-sectional, real-world study in 15.8 million adults. Diabetes Obes Metab. 2023 Nov;25(11):3390-3399.
[3] Couzin-Frankel J. Obesity meets its match. Science. 2023 Dec 15;382(6676):1226-1227.
[4] Andersen A, et al. Glucagon-like peptide 1 in health and disease. Nat Rev Endocrinol. 2018 Jul;14(7):390-403.
[5] Sharma D, et al. Recent updates on GLP-1 agonists: Current advancements & challenges. Biomed Pharmacother. 2018 Dec;108:952-962.
[6] Moon HS, et al. The development of non-peptide glucagon-like peptide-1 receptor agonist for the treatment of type 2 diabetes. Arch Pharm Res. 2011 Jul;34(7):1041-3.
[7] Muttenthaler M, et al. Trends in peptide drug discovery. Nat Rev Drug Discov. 2021 Apr;20(4):309-325.
[8] Aroda VR, et al. A new era for oral peptides: SNAC and the development of oral semaglutide for the treatment of type 2 diabetes. Rev Endocr Metab Disord. 2022 Oct;23(5):979-994.
[9] Best selling drugs of 2023. iPharmaCenter. 2023 Nov 3.
[10] Kalra S, et al. A Review on Semaglutide: An Oral Glucagon-Like Peptide 1 Receptor Agonist in Management of Type 2 Diabetes Mellitus. Diabetes Ther. 2020 Sep;11(9):1965-1982.
[11] Chao AM, et al. Semaglutide for the treatment of obesity. Trends Cardiovasc Med. 2023 Apr;33(3):159-166.
[12] Day JW, et al. A new glucagon and GLP-1 co-agonist eliminates obesity in rodents. Nat Chem Biol. 2009 Oct;5(10):749-57.
[13] Finan B, et al. A rationally designed monomeric peptide triagonist corrects obesity and diabetes in rodents. Nat Med. 2015 Jan;21(1):27-36.
[14] Coskun T, et al. LY3298176, a novel dual GIP and GLP-1 receptor agonist for the treatment of type 2 diabetes mellitus: From discovery to clinical proof of concept. Mol Metab. 2018 Dec;18:3-14.
[15] Coskun T, et al. LY3437943, a novel triple glucagon, GIP, and GLP-1 receptor agonist for glycemic control and weight loss: From discovery to clinical proof of concept. Cell Metab. 2022 Sep 6;34(9):1234-1247.e9.
[16] Wharton S, et al. Daily Oral GLP-1 Receptor Agonist Orforglipron for Adults with Obesity. N Engl J Med. 2023 Sep 7;389(10):877-888.
[17] Frias JP, et al. Efficacy and safety of oral orforglipron in patients with type 2 diabetes: a multicentre, randomised, dose-response, phase 2 study. Lancet. 2023 Aug 5;402(10400):472-483.